更多資訊
|
用于治療乳腺癌的靶向藥帕妥珠單抗國內獲批上市啦!时间:2018-12-27 作者:帕妥珠單抗國內獲批上市,用于治療乳腺癌!【原创】 阅读 我們知道乳腺癌是中國女性比較常見的惡性腫瘤,嚴重威脅女性的生命健康。據2012年國家腫瘤登記年報,全國女性乳腺癌發病率為十萬分之42.55,占女性全部腫瘤的16.81%,列為女性腫瘤發病率的第一位。乳腺癌中約有20%~30%的患者表現為HER2陽性,可導致患者臨床預后差,復發風險和死亡風險顯著增加。如今帕妥珠單抗國內獲批上市,給乳腺癌患者帶來了希望。
12月17日,國家藥品監督管理局批準乳腺癌創新靶向藥帕捷特®(英文名:Perjeta®,通用名:帕妥珠單抗)進口注冊申請,聯合曲妥珠單抗和化療,用于具有高復發風險的人表皮生長因子受體2(HER-2)陽性早期乳腺癌患者的輔助治療。
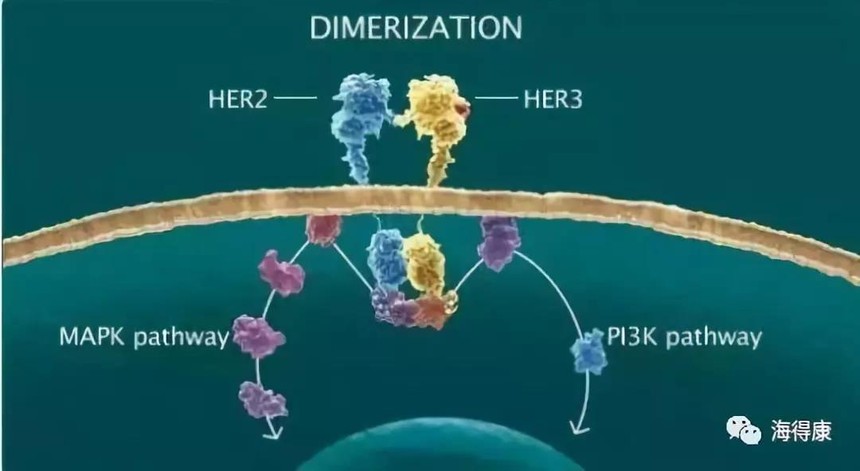
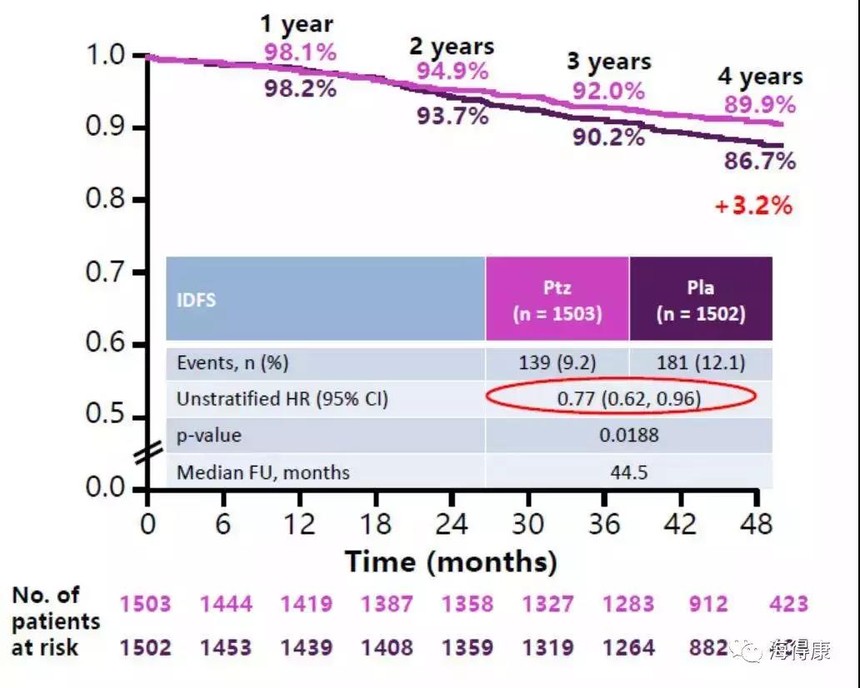
帕妥珠單抗(Pertuzumab,也被稱作2C4,商品名Perjeta)是一種單克隆抗體,是第一個被稱作“HER二聚化抑制劑”的單克隆抗體。通過結合HER2,抑制了HER2與其它HER受體的雜二聚,從而減緩了腫瘤的生長(百度)。由羅氏子公司Genentech研發,于2012年首次獲批。 曲妥珠單抗(商品名赫賽汀)是羅氏的另一個針對 HER-2 陽性乳腺癌的分子靶向治療藥物,1998年在美國上市,單藥治療已接受過1 個或多個化療方案的轉移性乳腺癌、或與紫杉醇/多西他賽聯合,用于未接受化療的轉移性乳腺癌患者。曲妥珠單抗已經在國內上市多年,去年進入醫保范圍。 帕捷特與赫賽汀雙靶治療方案,使具有高復發風險的 HER-2 陽性早期乳腺癌患者,復發或死亡風險降低 25%。目前,這種創新治療方案已在中國及國際多個指南和專家共識中被推薦,已經在全球超75個國家獲批。帕捷特在全球44個國家或是地區被納入醫保。 乳腺癌是女性發病率最高的惡性腫瘤。Her-2陽性乳腺癌是一類侵襲性強、惡性度高的乳腺癌亞型,HER-2陽性的早期乳腺癌患者接受赫賽汀聯合化療后,仍有約1/4的患者在10-11年后出現疾病復發或死亡,高危早期乳腺癌患者出現復發或死亡的比例更高。帕妥珠單抗與曲妥珠單抗同屬于靶向人表皮生長因子2受體(Her-2)的人源單克隆抗體藥物,區別在于二者對HER-2的作用位點不同,帕妥珠單抗與曲妥珠單抗聯合使用可以發揮更好的療效。 根據APHINITY研究的3期臨床研究顯示,與當前標準治療曲妥珠單抗聯合化療相比,使用帕妥珠單抗聯合曲妥珠單抗和化療用于具有高復發風險的HER2陽性早期乳腺癌患者輔助治療,復發風險降低23%。
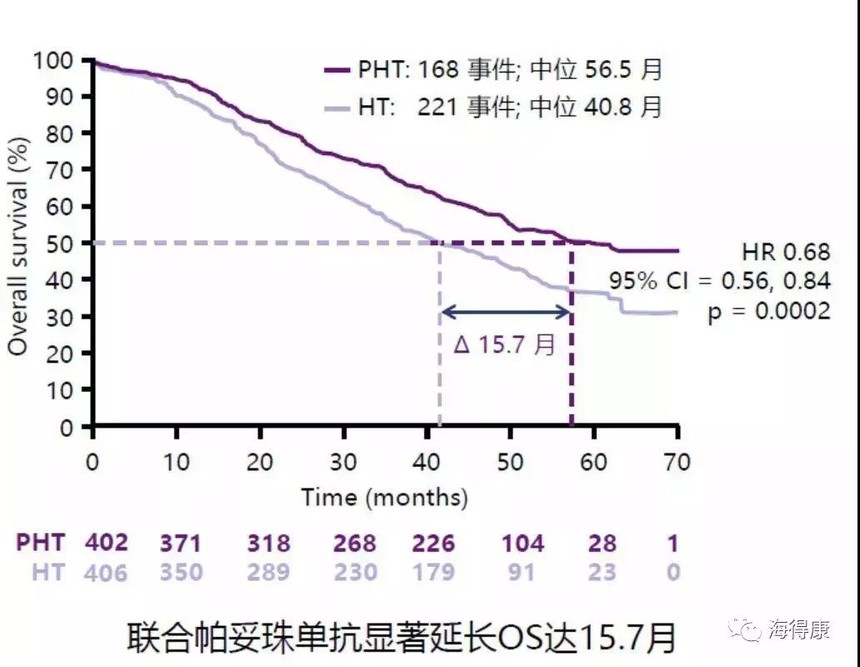
另外根據CLEOPATRA實驗顯示,對于晚期HER-2陽性乳腺癌患者,相比標準一線治療方案(使用曲妥珠單抗聯合化療),使用帕托珠單抗聯合曲妥珠單抗+化療可顯著延長總生存期15.7個月,患者總生存期可達56.5個月,接近5年。
在2012年6月被FDA批準聯合曲妥珠單抗和多西他賽用于未接受過抗HER-2療法或化療的轉移性乳腺癌。2013年9月FDA批準其聯合曲妥珠單抗和化療用于早期HER-2+乳腺癌的新輔助治療,在2017年12月被FDA批準聯合曲妥珠單抗和化療用于復發風險較高的早期HER-2陽性乳腺癌的輔助治療。“帕妥珠單抗+曲妥珠單抗+化療”聯合療法目前也已成為HER-2陽性乳腺癌患者的臨床治療金標準。 2017年國家癌癥中心數據統計:2014年中國女性乳腺癌新增病例27.89萬例。在進口抗癌藥零關稅、國家組織進行腫瘤藥醫保談判、多個國產曲妥珠單抗類似物接近申報上市的大背景下,帕妥珠單抗的獲批上市無疑會給中國乳腺癌患者提供更豐富的治療選擇。帕妥珠單抗獲得國家藥品監督管理局的審評并快速獲批,再次體現了國家對人民健康的關切。希望能有更多的乳腺癌創新產品更快地帶入市場,惠及廣大乳腺癌患者。 海得康由多年醫藥背景的海歸人員創辦,經過多番實地考察與國外大型醫院建立了官方合作關系。詳詢醫學顧問:400-001-9769,微信:HDK4000019769。 免責聲明:海得康不賣藥,只為患者提供出國就醫咨詢服務,用藥需由專業醫師指導。 |
|
|