更多資訊
|
替諾福韋二代(TAF)乙肝患者的長期治療藥物,印度也上市了仿制藥!时间:2020-06-01 作者:海得康官方咨詢電話:4000019769 阅读 隨著我國乙肝患者數量“破億大關”的完成,我國對于乙肝的治療達到了新的高度,最新引進了抗病毒藥物替諾福韋二代(TAF)用于乙肝的治療,TAF以其強效抗病毒、更高的轉氨酶復常率、更好的骨腎安全性、妊娠安全性、“零”耐藥等優點,得到臨床極大關注。 在TAF的全球Ⅲ期試驗中,使用TAF治療96周未檢出與TAF或TDF耐藥有關的位點置換,即未出現耐藥。研究表明,TAF治療144周,仍沒有檢測到與TAF耐藥有關的變異,即TAF治療144周保持“零”耐藥。
該研究針對的是TAF對比TDF全球Ⅲ期試驗的隊列,對于治療24周及以上、在144周時或提前停藥時HBV DNA仍≥69 IU/ml的所有患者,使用Illumina Mi-Seq深度測序法對乙型肝炎病毒(HBV)基因的pol/RT區測序,報告一致性序列水平變化15%以上的序列改變。 病毒學突破(VB)定義為獲得HBV DNA<69 IU/ml之后,2次檢測HBV DNA≥69 IU/ml或HBV DNA水平較最低水平升高1.0 log IU/ml或以上。對于依從試驗藥物[通過血漿替諾福韋(TFV)濃度判定]的VB患者、出現保守位點置換的患者或見于>1例患者的多態位點置換,進行體外表型分析。 9.9%的入組患者在末次訪視時符合測序標準,其中TAF治療人群(雙盲和開放標簽階段)10.4%,TDF治療人群(雙盲)7.5%。對所有患者(128例)的測序結果顯示,63例無序列改變、22例由于病毒載量過低而無法測序、31例有多態位點置換、12例有保守位點置換,保守位點的改變都不重復。144周時,3.5%(46/1298)的患者出現了VB(其中57%證實為不依從)。 這些患者的測序結果提示,他們的序列改變類型分布與整體隊列相似。另外,經治和初治患者的序列改變類型分布也是相似的。23例無法確定不依從試驗方案的VB患者接受了表型分析,結果顯示其對試驗藥物均敏感。對所有49例符合標準患者的表型分析均未檢測到TAF或TDF表型耐藥。這說明兩個藥物治療144周未產生耐藥。 耐藥機制的產生嚴重影響了患者們的治療,TAF創144周零耐藥記錄無疑是為患者們的長期治療提供了保障。
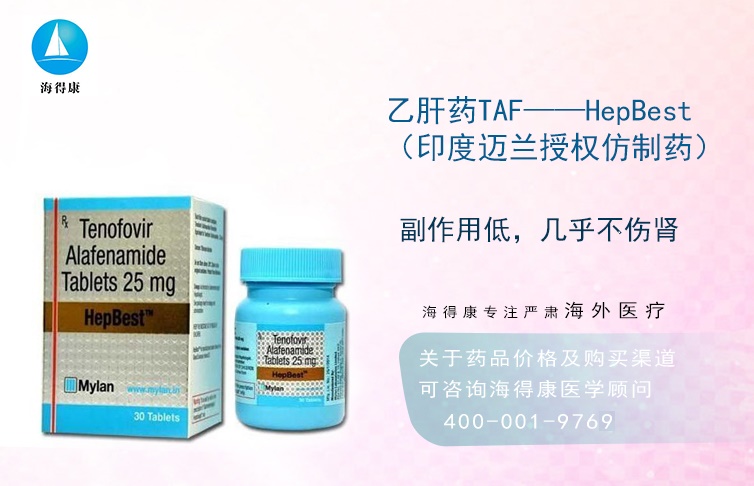
據了解,TAF仿制藥HepBest已在印度上市,由著名的邁蘭Mylan制藥授權(美國吉利德公司授權)仿制,與原研藥無二致。關于TAF(替諾福韋二代HEPBEST)更多問題,請咨詢官方電話:400-001-9769,微信號:15600654560,海得康醫學顧問會詳細為您解答疑問。 |
|
|