|
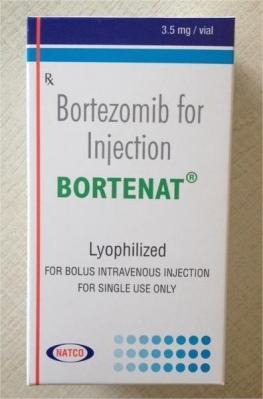
FDA批準Boruzu用于治療多發性骨髓瘤和套細胞淋巴瘤,仿制藥上市了嗎时间:2024-09-10 作者:醫學編輯李可艾 阅读 FDA已經正式批準了Boruzu,這是一種硼替佐米(Velcade)的新劑型,它既可以用于皮下注射,也可以用于靜脈注射,并且減少了傳統給藥方式所需的配制步驟。
作為一種蛋白酶體抑制劑,Boruzu被批準用于治療多發性骨髓瘤和套細胞淋巴瘤患者。與之前的Velcade凍干粉不同,Boruzu是即用型的,無需在使用前進行重構。 對于多發性骨髓瘤患者,Boruzu的推薦起始劑量為1.3 mg/m²,可以通過靜脈注射(濃度為1 mg/mL)或皮下注射(濃度為2.5 mg/mL)給藥。如果患者之前對硼替佐米有反應,并且在完成治療后至少6個月復發,那么可以考慮重新使用Boruzu進行治療。當選擇靜脈注射時,應以3至5秒的靜脈推注方式進行注射。 值得注意的是,Boruzu在臨床研究中報告了一些常見的毒性反應,包括虛弱、腹瀉、惡心、便秘、周圍神經病變、嘔吐、發熱、血小板減少、精神障礙、厭食和食欲不振、中性粒細胞減少、神經痛、白細胞減少和貧血等。因此,在使用Boruzu時,醫生和患者應密切關注這些潛在的不良反應,并采取相應的管理措施。
據悉,Boruzu的仿制藥已在印度正式上市。對于需要購買此藥的患者來說,現在有了更多的選擇。若考慮購買此藥,患者可以選擇前往國外就醫,并在當地合法購買該藥品。仿制藥為那些尋求更經濟、有效治療方案的患者帶來了希望。“海得康”作為一個專業的醫療咨詢平臺,有著豐富的國際新藥動態知識和經驗,能夠為國內患者提供全球已上市藥品的專業咨詢服務。如有需要,可以撥打服務熱線400-001-9769或海得康官方微信15600654560來獲取幫助。 請注意,所有關于藥物的使用和副作用的信息都應僅作為參考,具體用藥還請務必與醫生進行充分的溝通和討論。
|