|
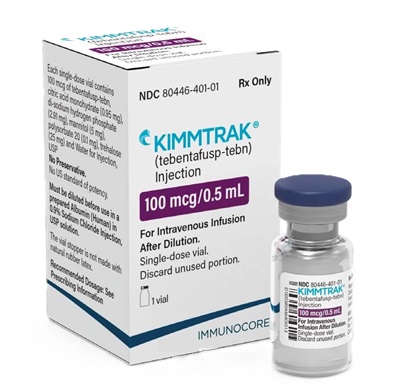
替本福司的全球使用現狀:哪些國家已批準上市?时间:2025-03-04 作者:醫學編輯李可艾 阅读 替本福司(tebentafusp)作為一種創新的雙特異性融合蛋白,已經在全球范圍內引起了廣泛關注。該藥物主要用于治療患有不可切除或轉移性葡萄膜黑色素瘤的HLA-A*02:01陽性成年患者。以下是關于替本福司全球使用現狀的詳細介紹,包括哪些國家已批準上市。 一、美國 替本福司于2022年1月在美國獲得食品藥品監督管理局(FDA)的批準上市,用于治療患有不可切除或轉移性葡萄膜黑色素瘤的HLA-A*02:01陽性成年患者。 該藥物在美國的上市為患者提供了新的治療選擇,并得到了臨床醫生和患者的廣泛認可。
二、歐洲 替本福司在歐洲的上市申請正在進行中,并已經獲得了歐洲藥品管理局(EMA)的優先審評資格。 盡管替本福司尚未在歐洲正式上市,但EMA的優先審評資格表明該藥物在歐洲市場的前景廣闊。 三、日本 替本福司在日本已經獲得了批準上市,用于治療患有不可切除或轉移性葡萄膜黑色素瘤的患者。 該藥物在日本的上市為患者提供了更多的治療選擇,并促進了當地黑色素瘤治療領域的進步。 四、其他國家與地區 除了美國、歐洲和日本外,替本福司在其他國家和地區的市場情況尚未明確公布。然而,隨著該藥物在全球范圍內的不斷推廣和應用,相信未來會有更多的國家和地區批準替本福司上市。 替本福司作為一種創新的治療藥物,已經在全球范圍內引起了廣泛關注。目前,該藥物已經在美國和日本獲得批準上市,并在歐洲獲得了優先審評資格。
海得康”發掘國際新藥動態,為國內患者提供全球已上市藥品的咨詢服務,更多問題,請咨詢海得康醫學顧問,電話:400-001-9769,海得康官網微信:15600654560。 【友情提示:本文僅作為參考意見。用藥期間隨時與醫生保持聯系,隨時溝通用藥情況。圖片侵權,請聯系刪除。】
|