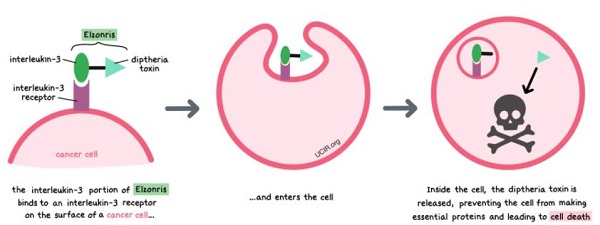
|
Elzonris(tagraxofusp-erzs)警告和注意事項时间:2022-09-15 作者:海得康醫學編輯劉曉曦【原创】 阅读 毛細血管滲漏綜合征 在接受ELZONRIS治療的患者中報告了毛細血管滲漏綜合征(CLS),包括危及生命和致命的病例。在臨床試驗中接受ELZONRIS的患者中,CLS的總體發生率為55% (52/94),其中1級或2級占46% (43/94),3級占6% (6/94),4級占1% (1/94) 和2起致命事件 (2/94, 2%)。ELZONRIS治療期間報告的與CLS相關的常見體征和癥狀(發生率≥20%)包括低白蛋白血癥、水腫、體重增加和低血壓。 在開始使用ELZONRIS治療之前,確保患者有足夠的心功能并且血清白蛋白大于或等于3.2g/dL。在使用ELZONRIS治療期間,在開始每劑ELZONRIS之前和之后根據臨床指示監測血清白蛋白水平,并評估患者CLS的其他體征或癥狀,包括體重增加、新發或惡化的水腫,包括肺水腫、低血壓或血流動力學不穩定。
超敏反應 ELZONRIS可引起嚴重的超敏反應。在臨床試驗中接受ELZONRIS的患者中,46% (43/94) 接受ELZONRIS治療的患者報告了超敏反應,并且在10% (9/94) 中為3級以上。≥5%的患者報告的超敏反應表現包括皮疹、瘙癢、口腔炎和喘息。在用ELZONRIS治療期間監測患者的超敏反應。如果發生超敏反應,中斷ELZONRIS輸注并根據需要提供支持性護理。 肝毒性 ELZONRIS治療與肝酶升高有關。在臨床試驗中接受ELZONRIS的患者中,88% (83/94) 的患者出現肝酶升高,包括48% (45/94) 的1級或2級,36% (34/94) 的3級,和4% (4/94) 中的4級。在每次輸注ELZONRIS之前監測丙氨酸氨基轉移酶 (ALT) 和天冬氨酸氨基轉移酶 (AST)。如果轉氨酶升高至大于正常上限的5倍,則暫時停止使用ELZONRIS,并在正常化或解決時恢復治療。 “海得康”發掘國際新藥動態,為國內患者提供全球已上市藥品的咨詢服務。海得康醫學顧問咨詢電話:400-001-9769,官網微信:15600654560。
【友情提示:本文醫藥信息內容僅供參考,具體疾病治療和用藥請咨詢醫生評估,海得康不承擔任何責任。本站圖片來源于網絡,侵權請聯系刪除。】 |