新聞中心
|
|
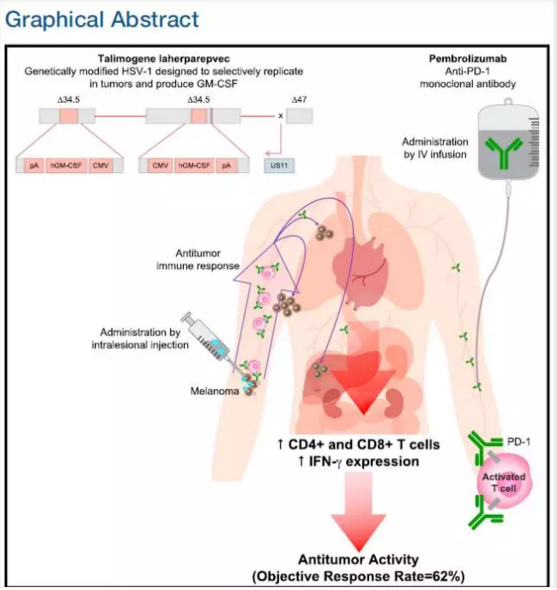
時間:2017-09-15 作者:PD1 【轉載】 Cell雜志上發表的一篇最新論文:Oncolytic Virotherapy Promotes Intratumoral T Cell Infiltration andImproves Anti-PD-1 Immunotherapy,該研究顯示,聯合使用溶瘤病毒藥物T-VEC(talimogene laherparepvec )和PD-1抗體藥物( pem-brolizumab)對黑色素瘤進行治療,腫瘤緩解率高達62%,其中33%為完全緩解。(Cell 170, 1109–1119, September 7, 2017)。 Pem-brolizumab,是美國FDA批準的第一個PD-1免疫檢測點抑制劑。pem-brolizumab證實在包括肺癌、腎癌、黑色素瘤、頭頸癌、膀胱癌、乳腺癌、肝癌、胃癌、食管癌、腦膠質瘤、結腸癌、霍奇金淋巴瘤等晚期癌癥治療方面有顯著療效,有望實質性改善患者生存期。 Talimogene laherparepvec,T-Vec是一種經過基因修飾的1型單純皰疹病毒(HSV-1),是FDA批準的第一個溶瘤病毒藥物,它可以在腫瘤細胞內復制并表達免疫激活蛋白粒細胞-巨噬細胞集落刺激因子(GM-CSF),加速抗腫瘤的免疫應答,主要用于晚期黑色素瘤的治療。 PD-1和PD-L1抗體由于其卓越的療效,正逐漸成為轉移性黑色素瘤、頭頸癌、肺癌、腎癌、膀胱癌以及默克爾細胞癌病人的標準治療方案,但隨著臨床實驗的進一步開展,發現并非所有的病人對PD-1抗體免疫治療都有積極響應,多數病人似乎先天對PD-1抑制劑療法耐受,而這些耐受病人的腫瘤內部往往缺少CD8+的T細胞。 研究人員推測,通過其他免疫療法促進CD8+的T細胞對腫瘤的浸潤也許能提高PD-1抗體的療效。于是設計了一個聯合用藥方案,先直接注射溶瘤病毒T-VEC到黑色素瘤病灶,再靜脈輸入PD-1抗腫瘤藥物(pem-brolizumab)。
在試驗開始時,患者腫瘤被注射了4mL x 10^6pfu/mL的T-Vec以誘導血清轉換和引起保護性免疫應答,3周之后再注射一次4mL x 10^8pfu/mL的T-Vec。從第6周開始,患者每兩周接受相同劑量的T-Vec瘤內注射以及200mg pem-brolizumab的靜脈注射。結果發現,在第6周時(2次T-Vec治療后,pem-brolizumab治療開始前),大多數腫瘤被浸潤了T細胞(下圖紅色部分)。在第30周時,T細胞依然保留在這一區域,但大部分腫瘤細胞消失了 參與這一次臨床試驗的21名轉移性黑色素瘤患者總緩解率為62%,其中,33%為完全緩解,意味著他們的腫瘤已經無法被檢測到。這一聯合療法的緩解率比單獨使用pem-brolizumab或T-Vec治療的預期緩解率(通常約為35%-40%)要高得多。證實了研究人員的推測,通過溶瘤病毒療法促進T細胞對腫瘤的浸潤確實能夠提高PD-1抗體的療效。 CD8 (green), and PD-L1 (red) ,S100 (blue,as melanoma segmentation marker) 令人欣喜的是,除了有效性的提升,這一研究中的副作用也沒有比單獨使用其中任何一種藥物帶來的副作用更糟,最常見的副作用為疲勞、寒顫和發燒。 盡管1b期臨床試驗顯示出了“pem-brolizumab+T-Vec”聯合療法的喜人前景,但是仍然需要更大規模的臨床試驗來確定其療效。 這是繼8月23日Science Translational Medicine雜志上發表的M1溶瘤病毒能高效殺傷腫瘤細胞后又一例證,再次顯示出了溶瘤病毒在腫瘤治療中的巨大潛力。 海得康發掘國際新藥動態,為國內患者提供全球已上市藥品的咨詢服務,如丙肝新藥印度吉三代、肝癌新藥印度多吉美、PD-1、PD-L1、肺癌AZD9291等,幫助國內患者選擇更新更有效的治療藥物和手段,更多藥品信息及購藥渠道,詳詢:400-001-9763,010-67385800,微信:headkonhdk m.jwxr.com.cn |
|
|